Early Career
Researchers若手研究者紹介
安間 太郎Yasuma Taro
医学部附属病院 講師
JST創発的研究支援事業2022年度採択

専門分野
免疫学、代謝内分泌内科学
所属学会等
日本免疫学会、日本内科学会(総合内科専門医)、日本糖尿病学会(専門医・指導医)、日本内分泌学会(専門医・指導医)
主な研究内容
臓器線維症は全身のあらゆる臓器で発生し、線維化を起こした臓器は、最終的に機能不全に陥る。臓器線維症は有効な治療法がなく、先進国において疾患関連死亡原因の45%を占めるといわれている。中でも糖尿病は世界で患者数が5億人を超え、糖尿病患者では高血糖を基盤としたさまざまな機序により臓器線維症が進行し、慢性腎不全や心血管疾患などの糖尿病合併症の主要な原因となっている。一方、近年、細菌叢の乱れが様々な疾患の発症に関与することが報告され、線維化の原因としても注目されているが、細菌叢の乱れが線維化を引き起こすメカニズムはほとんど分かっていない。
我々は肺線維症マウスから単培養された細菌の培養上清を解析することにより、細胞死を引き起こす細菌由来ペプチドであるcorisinを発見し(Nat Commun. 2020)、corisinを阻害することにより炎症・線維化が改善することを報告してきた(Nat Commun. 2022)。最近の実験ではcorisinが細胞死を誘導する以外にも様々な生理活性を有し、ヒトにおいても多様な疾患に関与することが分かってきた。我々の研究では、糖尿病を含む様々な疾患の動物モデルやヒトの検体を用いて細菌叢由来ペプチドの解析を行っており、将来的に細菌叢由来ペプチドを標的とした画期的な治療法を開発することを目指している。
主な研究内容に
関する概要図
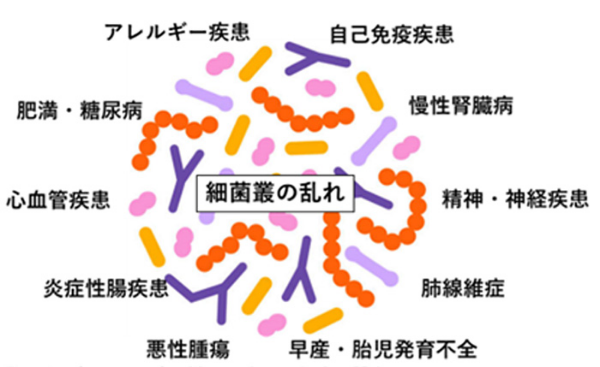
細菌叢の乱れ(dysbiosis)は様々な疾患の発症に関与することが分かっているがそのメカニズムは不明である。
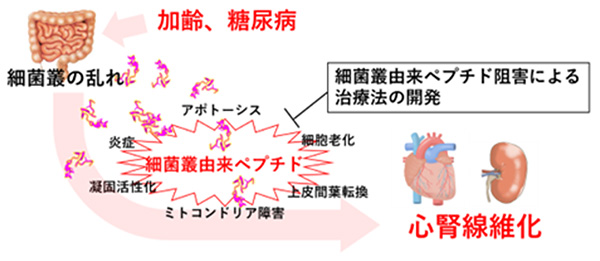
新たに細胞死と線維化を引き起こす細菌叢由来ペプチドを発見した。
現在、細菌叢由来ペプチドを標的とした新しい糖尿病心腎合併症の治療法開発を目指し研究を行っている。
研究業績
- 論文業績等
- Tsuruga T, Fujimoto H, Yasuma T, D'Alessandro-Gabazza CN, Toda M, Ito T, Tomaru A, Saiki H, Okano T, Alhawsawi MAB, Takeshita A, Nishihama K, Takei R, Kondoh Y, Cann I, Gabazza EC, Kobayashi T. Role of microbiota-derived corisin in coagulation activation during SARS-CoV-2 infection. J Thromb Haemost. 2024 Jul;22(7):1919-1935.
- Yasuma T, Gabazza EC. Cell Death in Acute Organ Injury and Fibrosis. Int J Mol Sci. 2024 Apr 1;25(7):3930.
- Nishiwaki R, Imoto I, Oka S, Yasuma T, Fujimoto H, D'Alessandro-Gabazza CN, Toda M, Kobayashi T, Osamu H, Fujibe K, Nishikawa K, Hamaguchi T, Sugimasa N, Noji M, Ito Y, Takeuchi K, Cann I, Inoue Y, Kato T, Gabazza EC. Elevated plasma and bile levels of corisin, a microbiota-derived proapoptotic peptide, in patients with severe acute cholangitis. Gut Pathog. 2023 Nov 30;15(1):59.
- Fridman D'Alessandro V, D'Alessandro-Gabazza CN, Yasuma T, Toda M, Takeshita A, Tomaru A, Tharavecharak S, Lasisi IO, Hess RY, Nishihama K, Fujimoto H, Kobayashi T, Cann I, Gabazza EC. Inhibition of a Microbiota-Derived Peptide Ameliorates Established Acute Lung Injury. Am J Pathol. 2023 Jun;193(6):740-754.
- D'Alessandro-Gabazza CN, Yasuma T(equal contribution), Kobayashi T, Toda M, Abdel-Hamid AM, Fujimoto H, Hataji O, Nakahara H, Takeshita A, Nishihama K, Okano T, Saiki H, Okano Y, Tomaru A, Fridman D'Alessandro V, Shiraishi M, Mizoguchi A, Ono R, Ohtsuka J, Fukumura M, Nosaka T, Mi X, Shukla D, Kataoka K, Kondoh Y, Hirose M, Arai T, Inoue Y, Yano Y, Mackie RI, Cann I, Gabazza EC. Inhibition of lung microbiota-derived proapoptotic peptides ameliorates acute exacerbation of pulmonary fibrosis. Nat Commun. 2022 Mar 23;13(1):1558.
- Saiki H, Okano Y, Yasuma T(equal contribution), Toda M, Takeshita A, Abdel-Hamid AM, Fridman D'Alessandro V, Tsuruga T, D'Alessandro-Gabazza CN, Katayama K, Sugimoto M, Fujimoto H, Yamanaka K, Kobayashi T, Cann I, Gabazza EC. A Microbiome-Derived Peptide Induces Apoptosis of Cells from Different Tissues. Cells. 2021 Oct 26;10(11):2885.
- D'Alessandro-Gabazza CN, Kobayashi T, Yasuma T(equal contribution), Toda M, Kim H, Fujimoto H, Hataji O, Takeshita A, Nishihama K, Okano T, Okano Y, Nishii Y, Tomaru A, Fujiwara K, D'Alessandro VF, Abdel-Hamid AM, Ren Y, Pereira GV, Wright CL, Hernandez A, Fields CJ, Yau PM, Wang S, Mizoguchi A, Fukumura M, Ohtsuka J, Nosaka T, Kataoka K, Kondoh Y, Wu J, Kawagishi H, Yano Y, Mackie RI, Cann I, Gabazza EC. A Staphylococcus pro-apoptotic peptide induces acute exacerbation of pulmonary fibrosis. Nat Commun. 2020 Mar 24;11(1):1539.
- 外部資金獲得状況(科研費等)
-
代表者として獲得した公的研究助成
- 科研費若手研究(2019-2020年度)
- 科研費若手研究(2021-2022年度)
- 科研費基盤C(2024-2026年度)
- JST創発的研究支援事業(2023-2029年度)
-
代表者として獲得した主な民間の研究助成
- 日本糖尿病財団 第2回ノボノルディスクファーマ研究助成(2022年)
- 鈴木謙三記念科学応用財団 2022年度調査研究助成(2022年)
- 武田科学振興財団 2022年度医学系研究助成基礎(2022年)
- 興和生命科学振興財団 研究助成(2021年)
- グラクソスミスクラインジャパン研究助成(2021年)
- 難病医学研究財団 医学研究奨励助成(2021年)
- 日本糖尿病協会 2016年度若手研究者助成(2016年)